
QIAGEN宿主细胞残留完整解决方案
CGT领域的高速发展得到了国家药监局的高度重视,该领域被认为是未来医药领域发展的潜力。早在2010年FDA 发布的生物制品相关指导中,指名“终产品中需要检测残留 DNA 的含量和片段大小分布情况”。截止目前研究表明,一个功能基因至少在 200bp 以上,因此,为减少残留 DNA 风险,残留的片段不大于 200bp。
1.
2022年5月份在国家药品监督管理局部署下,药审中心发布了《体内基因治疗产品药学研究与评价技术指导原则(试行)》中,首次将风险性DNA残留片段的大小控制在200bp以下进行明文规定:建议尽量将残留DNA控制在10ng/剂以内,DNA残留片段的大小控制在200bp以下。 |
宿主细胞残留核酸检测难点如下:1)高效的提取到残留核酸,如何提高微量核酸的提取回收率。2)建立一种快速的检测方法,以检测残留核酸的浓度以及其片段分布情况。凯杰(QIAGEN)作为分子领域全流程完整解决方案供应商,提供残留核酸检测方案如下,助您轻松提高实验室检测效率。
01
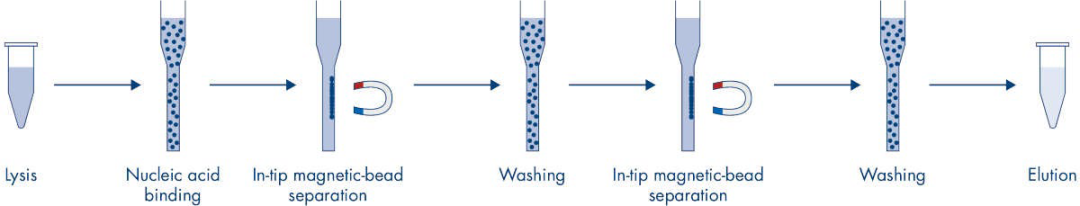
残留核酸提取仪——EZ2 Connect

保障微量残留核酸的提取效率,速度快,安全性能强,有效避免交叉污染。


通量灵活,1-24样本
速度快,最快16分钟可完成24个样本的纯化
配备加热模块,实现自动化加热孵育等流程
内置试剂条开封装置,机内开封提高安全性
最新的图形用户界面,便于使用
可根据需要生产报告进行数据跟踪
预安装程序可以方便选择启动
具备满足21 CFR Part 11审计追踪功能
嵌入式紫外灯,可随自动加样臂在机器内部各个角落自由移动
配套预装试剂
.
无需担心试剂开封后效期
不浪费试剂耗材
灵活的上样体积: 大至8 ml
支持大体积游离核酸提取
FFPE和cfDNA提取优势
02
自动化残留核酸质控设备——QIAxcel Connect
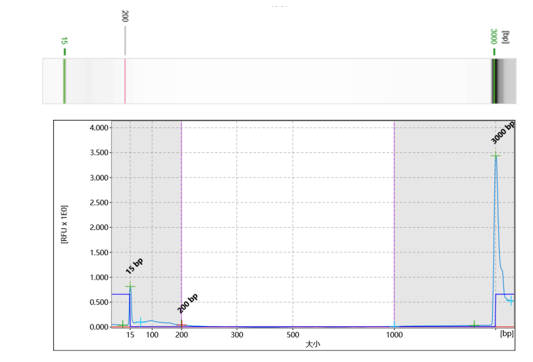
建立了快速有效的残留核酸片段分布的检测方法,轻松给出小于200bp片段的占比。


多达96个样品的快速分析,无需人工干预
即用型预制凝胶卡夹安全且方便
浓度低至5 pg/μlDNA核酸样品
(50pg/μl RNA)的高灵敏性检测
标准且准确的分析,分辨率可达3-5bp
界面友好的中/英文分析软件
支持 21 CFR第11部分的合规要求
配套预装试剂
.
每次样品消耗量小于0.1ul
预制凝胶卡夹,可满足不同的分辨率,
灵敏度和速度要求。